OTS、新生血管阻害剤 OCV-101 第Ⅱ相臨床試験開始
オンコセラピーサイエンスが2月1日、大塚製薬と共同で新生血管阻害剤OCV-101の第Ⅱ相臨床試験を開始すると発表しました。OCV-101はOTS11101のコード名を今回の試験より変更したもの。
平成 23 年 2 月 1 日
各 位
神奈川県川崎市高津区坂戸3-2-1
オンコセラピー・サイエンス株式会社
代表取締役社長 角田 卓也
(問い合せ先)取締役管理本部長 山本 和男
電話番号 044‐820‐8251
新生血管阻害剤 OCV-101 第Ⅱ相臨床試験開始のお知らせ
当社が大塚製薬株式会社と契約を締結し、共同で開発を進めております新生血管阻害剤 OCV-101(旧「OTS11101」。本試験より治験薬コード名変更。)の膵臓がんに対する第Ⅱ相臨床試験を開始しますので、お知らせいたします。
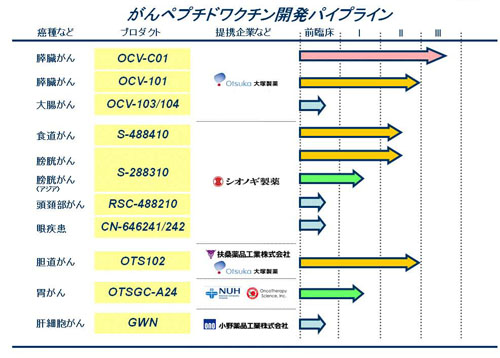
新生血管阻害剤 OCV-101 は、腫瘍新生血管内皮細胞を標的とするがんワクチン療法剤です。 開始いたします臨床試験は、切除不能進行膵臓がん及び再発膵臓がんの患者さんを対象とし、その有効性及び安全性を確認する第Ⅱ相臨床試験です。本試験は全国 8 施設で施行いたします。
当社は、この治験開始に伴い、大塚製薬から契約に基づくマイルストーンを受領いたします。
なお、本件は当初計画に含まれており、発表済みの通期予想に変更はありません。
以 上
OTS-102との違いはペプチドが異なるということでしょうね。同じ新生血管阻害剤ですが、詳しい情報を探し当てられませんでした。「全国8施設」はどこか。中村教授のwebにいずれ発表されると思われます。OTS-102はこんな説明です。
腫瘍の継続的な増殖や転移には,血管新生が重要な役割を果たしています。その血管新生を促進する最も強力な物質のひとつが血管内皮増殖因子(vascular endothelial growth factor:VEGF)であり,その主要なシグナル伝達を担う主要な受容体は血管内皮増殖因子受容体(vascular endothelial growth factor receptor:VEGFR)-2/キナーゼドメイン受容体(kinase domain receptor:KDR)であることが知られています。 KDRを特異的に認識する細胞傷害性T細胞(cytotoxic T lymphocyte:CTL)を誘導できる数種類のHLA-A*2402拘束性エピトープペプチドのうち,最も強いCTL誘導能をもつペプチドが KDR169です。
本治験で用いるOTS102は有効成分としてKDR169を含有する注射剤です。OTS102をHLA-A*2402を有する癌患者に皮下投与することにより,有効成分であるKDR169が抗原提示細胞のHLAに結合しCD8陽性細胞に提示され,これを認識したT細胞が活性化されてKDR特異的CTLが誘導されます。誘導されたCTLはKDRを発現している腫瘍新生血管内皮細胞を特異的に傷害し,これにより抗腫瘍効果を示します。







はじめまして。
2年前に母を膵臓ガンで亡くした者です。
母は、病名が分かってから3ヶ月で亡くなってしまいまして、今もまだ気持ちの置き所がありません。
本日、以下のイベントの説明会に参加してきまして、まだまだ告知が足りないと実感致しました。
よろしければ、こちらのサイトでも紹介して頂けたら幸いです。
よろしくお願い致します。
「パープルリボンウォーク」が東京で初めて開催されます。
開催日: 2011 年6月11日(土)雨天決行
集合: 日比谷公園大噴水前
種目: 2キロコース 5キロコース
参加費:大人1000円(当日1500円) 小・中学生500円(当日800円)
参加申し込み及び詳細確認は以下のURLからどうぞ
さして情報価値はありませんが、全国8施設については公開はしない方針ながらも、地方別の情報は貰えまして、北海道、東京(関東)、東海、関西の4地方だそうです。具体的にどの施設かは(東京の一つは判明済みのようですが)主治医を通せば分かる(はず)との回答でした。(O製薬の広報部)
ビタチョコ様、情報ありがとうございます。
あとの7カ所はたぶん中村教授のリストに載っている病院の中から選ばれるのでしょうね。関東で3カ所、関西2、東北1、中国1といったところでしょうか。予想ですが。
キノシタさま
はじめまして。
主人が膵がんで闘病中です。(50代前半ステージⅣa手術不適応)
昨年6月以来こちらを拝見させて頂いております。
情報を発信して頂きたいへんありがたく思っております。
さて新生血管阻害剤 OCV-101 の臨床試験についてですが、夫の担当医師に尋ねたところこちらの病院でも行うそうです。
こちらとは築地市場の前に位置する病院です。
1/8が当病院となります。
(医師によると臨床試験の条件は初回治療と。
後その医師の私見ですが「まだ夢のような結果がでるものではないと思っている」そうです。)
直にわかるでしょうが、とりあえずお知らせしますね。
陶さん。お久しぶりです。術後すでに1年10ヶ月経過したのだと思いますが、いかがですか? 2年経てば相当再発のリスクは小さくなると思います。しかし、この病気特に膵がんは、いつまで経っても不安はなくなりません。
今度の臨床試験は施設も公表しないということですか。UMINにも登録はされないのでしょうね。もっとも臨床試験に登録の義務はありませんから、致し方ないです。アメリカでは全ての臨床試験登録を義務化しようとする動きもあるようですが、アメリカでさえですから、日本ではまだまだ先の話でしょう。
情報が入手できましたらコメントをお願いします。
いつもながら貴重な情報をお知らせ頂き有難とうございます。
今回のOCV-101の治験はオンコセラピーサイエンス社ではなく大塚製薬主導だそうで
(つまり、オンコセラピーサイエンスは治験参加には直接的な関わりをもたないようです)
かつまた、8つの施設についてもどこなのか公開はされないそうです。
大学病院の連携センターや主治医を通して治験のネットワークに連絡をして参加の
可否を探るという手立てをとる必要があるとのことです。