リキッド・バイオプシーを治験で受けるには?
ーー 目次 --
先日12月12日の「『膵臓がん患者と家族の集い』 Web 交流会」では、リキッドバイオプシーの話題も盛り上がりました。
「民間のリキッド・バイオプシー検査は高額だよね」との発言がきっかけでした。
「使える抗がん剤がもうありません」と言われても、まだがんゲノム医療があります。遺伝子の変異があってそれに対して効果のある薬が使えるようであれば、治療に結びつけることができます。
しかし、それには腫瘍の遺伝子検査が必要なのですが、一定量の組織のサンプルが必要でした。手術のできた患者ではプレパレートに保存されている組織が使えることもありますが、手術不可の患者はその方法が使えません。
遺伝子検査のためにわざわざ膵臓に針を刺してがん細胞取ってくるということには、がん細胞を撒き散らすというリスクがあります。また、必ずしもすべての患者さんががんの組織を採取できるとも限りませんでした。
リキッド・バイオプシーが実用段階に
しかし最近、血液から遺伝子の変異を見つける技術(リキッド・バイオプシー)が急速に進歩して実用段階になってきました。
それを報告したのが国立がん研究センター東病院のこちらの論文です。
- 国立がん研究センター東病院は、消化器がんにおいて、血液を用いてがんのゲノム異常を検出する検査(リキッドバイオプシー)を治験のスクリーニングに取り入れた
- その結果、従来の腫瘍組織検査に比べてより迅速に検査結果が返却され、より多くの患者さんが治験に登録された。
- リキッドバイオプシーが腫瘍組織検査と比べ、約22日早く解析結果が判明し、さらにゲノム解析結果に基づき、対応する治療薬の治験に登録した患者さんの割合が高まる
これまでの経過
- 2014年2月より、「SCRUM-Japan(スクラム・ジャパン)」を立ち上げ、「GI-SCREEN-Japan」に取り組んできました。
- GI-SCREEN-Japanは、国内の主要ながん専門病院や大学病院と協働して、進行消化器がんの患者さんの腫瘍組織を遺伝子パネル検査(Oncomine Comprehensive Assay)で解析し、治療薬を届ける全国がんゲノムスクリーニングプロジェクトです。
- 2018年1月より、GI-SCREEN-Japan(現:MONSTARーSCREEN)の基盤を活用し、進行消化器がんの患者さんの血液をリキッドバイオプシーで解析するスクリーニングプロジェクト「GOZILA Study」を開始しました。
腫瘍組織検査とリキッド・バイオプシー検査の比較
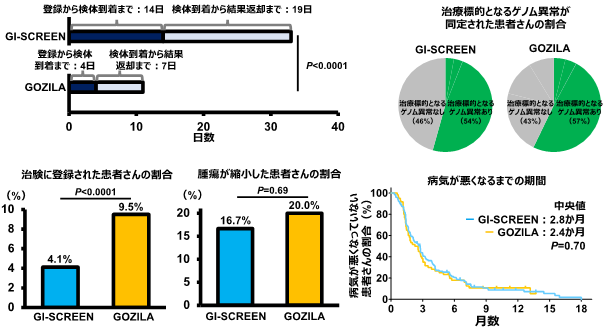
本研究では、GI-SCREEN-Japan(腫瘍組織検査)に登録された5743例と、GOZILA Study(リキッドバイオプシー)に登録された1787例を比較しました。その結果、
- プロジェクト登録後~検体到着までの期間(中央値:14日 vs. 4日、P<0.0001)
- 検体到着後から解析結果が患者さんに返却されるまでの期間(中央値:19日 vs. 7日、P<0.0001)
- 治療標的となるゲノム異常が同定された患者さんの割合(54% vs. 57%)
- ゲノム異常に適合した薬剤の治験に登録された患者さんの割合(4.1% vs. 9.5%、P<0.0001)
- 治験治療で腫瘍が縮小した患者さんの割合(16.7% vs. 20.0%、P=0.69)
- 治験治療で病気が悪くなるまでの期間(中央値:2.8か月 vs. 2.4か月、P=0.70)
と、ほとんど差がない結果となりました。
腫瘍組織がない患者でもゲノム検査を受けることができるのです。
治験に参加して、ゲノム検査を受ける
リキッド・バイオプシーの検査は民間でもやられているようです。
しかし50から150万円ほどの費用がかかると言われています。しかもその結果が遺伝子の異常を検出できるとも限らず、遺伝子異常が検出されても、それに合う薬が使えるかどうかは分かりません。
ですから高額な費用を出して検査することには躊躇するかもしれません。しかしこちらの臨床試験や医師主導の治験に参加すれば、検査費用は無料で受けることができます。
SCRUM-Japanの治験に参加するには

国立がん研究センター東病院のサイトにある「SCRUM-Japan」のページから、「MONSTAR-SCREEN」を選んでいくと、「患者さん向けの参加方法」があります。
「MONSTAR-SCREEN」の実施基盤で行っている治験が「GOZILA Study」です。
参加条件
- 大腸がん(直腸がん、結腸がん含む)、胃がん、食道がん、肝細胞がん、胆道がん(胆のうがん、肝内胆管がん含む)、膵がん、小腸がん(十二指腸がん含む)、虫垂がん、肛門管がん、消化器原発の神経内分泌腫瘍/癌(NET,NEC,MANEC)、消化管間質腫瘍GIST、乳がん、皮膚がん(悪性黒色腫、メルケル細胞がん)、頭頸部がん、前立腺がん、腎盂がん、尿管がん、膀胱がん、腎細胞がん、卵巣がん、卵管がん、腹膜がん、子宮体がん、子宮頸がん、原発不明がん(一部)のいずれかである。
- 手術が不可能もしくは再発している。
- 16歳以上である。
- Eastern Cooperative Oncology Group performance status(PS)が0-1。
- 登録前21日以内の最新の臨床検査値(登録日の21日前の同一曜日の検査値は可)が、以下のすべてを満たす。
- AST,ALT :≦100 U / L(肝転移を有する症例では各々≦200U/L)
- 総ビリルビン :≦正常上限値x1.5(閉塞性・体質性黄疸合併例は、≦3.0mg/dLまで)
- クレアチニン :≦1.5 mg/dL
- 重篤な併存疾患を有しない(例:コントロール不良な糖尿病や感染症、症状のある間質性肺炎や肺線維症など)。
- 登録日から12週以上の生存が期待される。
- 遺伝子異常の結果に応じた研究的な治療を受ける意思がある。
- 以下のいずれかに該当する。
- 薬物療法未治療である
- 特定の遺伝子異常を持っている
- 免疫チェックポイント阻害剤による治療を予定している
- 特定の分子標的薬による治療を予定している
受診手順
- 「MONSTAR-SCREEN」参加施設から膵臓がん患者を受け付けている病院を探す
- 該当する診療科宛の紹介状の作成を主治医に依頼する
- 医療機関への予約を取ってから紹介状をもって「初診」として受診する(セカンドオピニオンではないので注意)
- 予約時の電話で「MONSTAR-SCREEN(モンスター・スクリーン)やゲノム医療」と言っても通じません。診察時に医師にお伝えください。
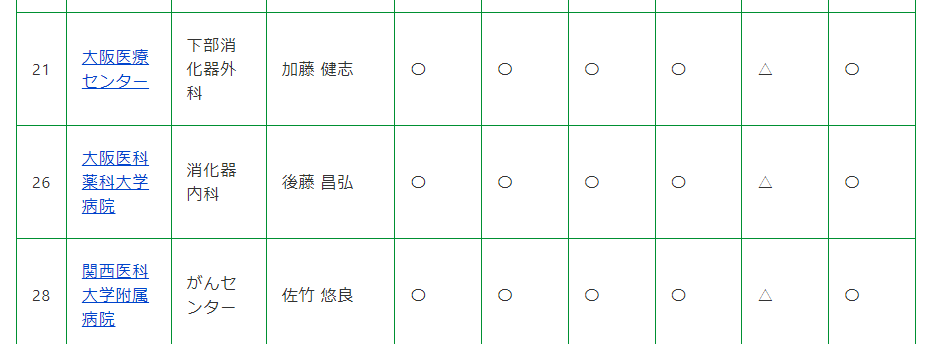
「MONSTAR-SCREEN」参加施設
中国、四国、九州は少ないですね。がん治療の均てん化もまだまだ満足できる状況ではないです。
リストの肝胆膵の欄はすべて△**となっていて、「△**:胆道がん・膵臓がん登録中断中」ですが、
・膵臓がんは2020/11/6~且つVer4.0IRB承認後、一次治療前原則60歳以下登録開始
(IRB:治験承認委員会のことです)
とありますので、主治医に確認してもらった方がよろしいでしょう。
治験を受けた患者のブログ
実際に国立がんセンター中央病院の患者で治験を受けられた方のブログがあります。